Enzimas: Relación Estructura-Función
Objetivo Fundamental:
- Comprender los principios básicos de la estructura de las enzimas para explicar el funcionamiento de los seres vivos.
Aprendizajes Esperados:
- Apreciar la importancia de las enzimas como catalizadores biológicos y como incide su estructura en su función.
Objetivos Fundamentales Transversales (O.F.T):
- Promover el interés y capacidad de conocer la realidad.
- Manejar herramientas de programas computacionales y redes de comunicación para el acceso a información especifica.
Las enzimas están en el centro de cada proceso bioquímico. Actuando en secuencias organizadas catalizan cientos de reacciones consecutivas mediante las que se degradan nutrientes, se conserva y transforma la energía química y se fabrican las macromoléculas biológicas a partir de precursores sencillos. A través de la acción de las enzimas reguladoras las rutas metábólicas están altamente coordinadas, proporcionando una armoniosa influencia recíproca entre la multitud de actividades diferentes que son necesarias para la vida.
Con la excepción de un pequeño grupo de moléculas de ARN catalítico todas las enzimas son proteínas. Su actividad catalítica depende de la integridad de su conformación proteica nativa. Si se desnaturaliza o se disocia una enzima en sus subunidades, se pierde normalmente la actividad catalítica si se descompone una enzima en sus aminoácidos constituyentes siempre se destruye su actividad catalítica. Así, las estructuras primarias, secundarias, terciarias y cuaternarias de las proteínas enzimáticas son esenciales para su actividad catalítica.
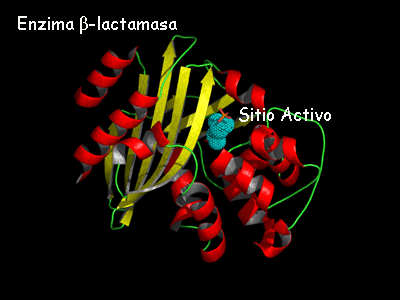
Propiedades de las enzimas:
- Catalizadores orgánicos: aceleran la velocidad de las reacciones bioquímicas, sin ser alteradas químicamente por la reacción que catalizan. Debido a esto último, las enzimas pueden actuar varias veces y, por lo tanto, resultan efectivas aún en cantidades muy pequeñas.
- Energía de activación: las energías de activación son barreras energéticas para las reacciones químicas, estas barreras son cruciales para la propia vida. Sin tales barreras energéticas, las macromoléculas complejas revertirían espontáneamente a formas moleculares muchos mas sencillas. No podrían existir ni las estructuras complejas y altamente ordenadas ni los procesos metabólicos que tienen lugar en cada célula. Las enzimas son moléculas que están para disminuir la energía de activación de las reacciones necesarias para la supervivencia celular. En los laboratorios químicos, también es frecuente que la energía de activación sea proporcionada por el calor. Cuando se aplica la llama de un mechero al matraz que contiene las sustancias reactantes, las moléculas de estas aceleran sus movimientos, lo que se traduce en un aumento de colisiones moleculares que favorecen las reacciones químicas. En las células vivas, un incremento del calor aceleraría igualmente todas las reacciones metabólicas, pero, muy pronto las proteínas se desnaturalizarían, perderían su funcionalidad y aparecerían otros efectos destructivos.
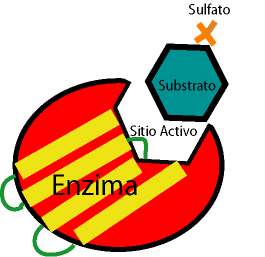
- Formación de un complejo enzima-sustrato: Las enzimas controlan las reacciones bioquímicas ofreciendo un entorno tridimensional a los reactivos sobre los que actúan. Toda molécula de enzima posee un sitio, denominado sitio activo, donde tiene lugar su acción catalítica. El concepto de sitio activo de una enzima corresponde a una depresión o hendidura relativamente pequeña que posee la geometría y distribución de cargas (positivas y negativas) para unirse específicamente y en forma complementaria a un determinado sustrato, (este sitio activo es el lugar donde a través del reconocimiento molecular ocurren las reacciones de ruptura y formación de enlaces) formándose así un complejo enzima-sustrato en el que las moléculas de las sustancias reactantes (sustratos) quedan muy próximas entre si, condición indispensable para que se lleve a cabo la reacción química de ellas. Por ultimo cabe señalar que, al separarse los productos de la enzima, esta ultima queda libre e intacta para catalizar la biosíntesis de nuevos productos iguales a los anteriores.
- Especificidad: cada una de las enzimas cataliza una sola reacción química o en ciertos casos unas pocas reacciones íntimamente relacionadas, por la similitud molecular de los sustratos.
Regulación de la actividad enzimática:
- Concentraciones: si aumenta la concentración de sustrato o de la enzima, la velocidad de la reacción también crece; en otras palabras, a mayor cantidad de sustrato o enzima, mas grande es la elaboración de producto, en un tiempo dado. En algunas ocasiones ciertas células pueden disponer abundantemente de un sustrato definido, y no poseer la cantidad adecuada de la enzima específica para ese sustrato. La enzima, en tal caso, constituye un factor limitante del metabolismo celular en aquellas células.
- Inhibores: Ciertas moléculas pueden inhibir la acción catalítica de un enzima: son los inhibidores. Estos inhibidores bien pueden ocupar temporalmente el centro activo por semejanza estructural con el sustrato original (inhibidor competitivo) o bien alteran la conformación espacial del enzima, impidiendo su unión al sustrato (inhibidor no competitivo).
- Desnaturalización: Cuando las proteínas se desnaturalización pierden su nivel terciario de organización y, consecuentemente, dejan de funcionar. En el caso particular de las enzimas , tres condiciones ambientales pueden determinar que las enzimas pierdan su funcionalidad como consecuencia de la desnaturalización:
- pH: las enzimas tienen un pH óptimo o un intervalo de pH en el que su actividad es máxima; a valores inferiores o superiores de pH la actividad disminuye. Esto no es sorprendente dado que algunas cadenas laterales de aminoácidos pueden actuar como ácido o bases débiles que desarrollan funciones críticas en el sitio activo de la enzima, que dependen de su mantenimiento en un cierto estado de ionización. Por otra parte las cadenas laterales ionizadas de la proteína pueden jugar un papel esencial en las interacciones que mantiene la estructura de la proteína.
- Temperatura: En general, los aumentos de temperatura aceleran las reacciones químicas: por cada 10ºC de incremento, la velocidad de reacción se duplica. Las reacciones catalizadas por enzimas siguen esta ley general. Sin embargo, al ser proteínas, a partir de cierta temperatura, se empiezan a desnaturalizar por el calor. La temperatura a la cual la actividad catalítica es máxima se llama temperatura óptima. Por encima de esta temperatura, el aumento de velocidad de la reacción debido a la temperatura es contrarrestado por la pérdida de actividad catalítica debida a la desnaturalización térmica, y la actividad enzimática decrece rápidamente hasta anularse.
- Metales pesados: los iones de algunos metales pesados, tales como el plomo (Pb ) y el mercurio ( Hg ), precipitan a las proteínas y, por lo tanto inactivan las enzimas. Normalmente, las enzimas están en suspensión dentro del citoplasma o unidas a una biomembrana. Si los iones de un metal pesado se combinan con una enzima en suspensión, la molécula proteica precipita, perdiendo su eficacia como enzima.
Actividades:
- ¿Cómo es que la estructura de la enzima puede incidir en su función? Discute junto a tu grupo de trabajo.
- ¿A qué corresponde el sitio activo?
- Ingresa a la base de datos descarga una enzima e identifica el sitio activo (ayudate con los tutoriales).
![]()
Copyright(c) 2003