| Ejercicio 2 | |
|
La
configuración electrónica de un elemento es:
1s2 2s2 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p5 Indíquese:
|
|
| Solución | |
|
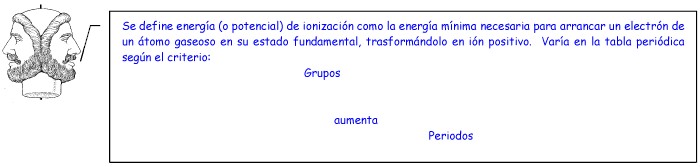
a) Se trata de un no metal, pertenece al grupo de los halógenos y su símbolo es I (iodo). b)
Elementos con mayor energía de ionización: cloro y bromo (los que estén encima de él en el grupo) Elementos con menor energía de ionización: rubidio y estroncio (los que estén a su izquierda en el periodo)
c) Compuesto iónico: buscaremos un elemento muy electropositivo para que la diferencia de electronegatividad sea muy grande, de modo que garantice el carácter metálico del enlace: por ejemplo " KI (ioduro potásico) Compuesto covalente: buscaremos un elemento que no difiera mucho de la electronegatividad del iodo. por ejemplo " IF5 (pentafluoruro de iodo)
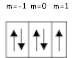
d) Electrón 5p5. n = 5 ; l = 1 ; m = 0 ; s = -1/2
|
|