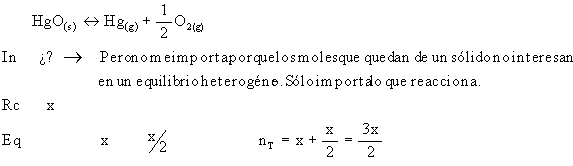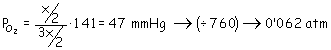| Ejercicio 21 | |
Cuando
el óxido mercúrico (sólido) se calienta en un recipiente cerrado
en el que se ha hecho el vacío, se disocia reversiblemente en
mercurio y oxígeno hasta alcanzar una presión total que en el
equilibrio vale a 380ºC 141 mmHg. Calcúlese
DATO: punto de ebullición del mercurio 357ºC. |
|
| Solución | |
|
a)
b)
c)
|
|