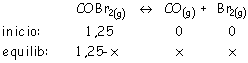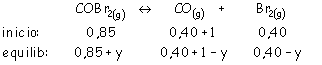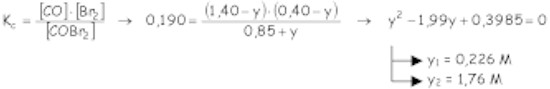| Ejercicio 12 | |||
En
un recipiente que tiene una capacidad de 4 litros, se introducen 5
moles de COBr2 y se calienta hasta una temperatura de 350ºK.
Si la constante de equilibrio de disociación del COBr2
en monóxido de carbono y bromo es 0,190 mol/l, determine:
|
|||
| Solución | |||
|
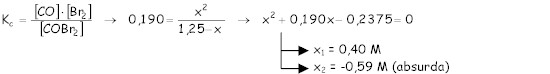
a) Concentración inicial COBr2 = 5/4 = 1,25 M.
b) Al añadir una concentración de 4/4 = 1 M, por el principio de Le Chatelier se desplazará el equilibrio hacia la izquierda:
El segundo valor de "y" es absurdo porque no puede desaparecer más CO del que hay. Por tanto las concentraciones en estas condiciones serán: c) Hacia la izquierda. |
|||