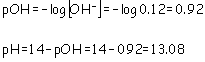| Ejercicio 13 | |
|
Calcule la riqueza, expresada en % y el pH de una disolución de hidróxido de calcio sabiendo que su densidad es 1.02 g/cc y que para neutralizar 25 ml de la misma necesitamos 30 ml de una disolución de ácido clorhídrico 0.1 M. |
|
| Solución | |
|
Calculemos en primer lugar el HCl contenido en los 30 ml de disolución 0.1 M:
La reacción: 2HCl + Ca(OH)2 " CaCl2 + 2H2O Así, los moles de HCl reaccionarán con la mitad de Ca(OH)2, esto es, 1.5 10-3 moles o bien como 1.5 10-3 mol 74.1 g/ml = 0.11 g de Ca(OH)2. Los 0.11 g se encuentran en 25 ml, es decir, en un peso de disolución de 25ml 1.02g/ml=25.5 g de disolución.
La riqueza de la disolución será:
Nº moles de OH- = 2 nº moles Ca(OH)2 = 2 1.5 10-3 = 3 10-3 moles. Para calcular [OH-] "
|
|