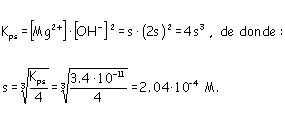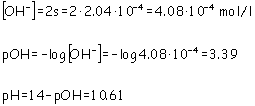| Ejercicio 11 | |
|
Se saturan 500 ml de agua con hidróxido de magnesio. Calcular el pH de la disolución resultante. DATO: Kps = 3.4 10-11 (no considerar el equilibrio de autodisociación del agua). |
|
| Solución | |
|
Equilibrio de solubilidad: Mg (OH)2 (s) D Mg2+(aq) + 2OH-(aq) Por cada mol de Mg(OH)2 que se disuelve se produce 1 mol de iones Mg2+ y 2 moles de iones OH-. La solubilidad, s (mol/l), será:
|
|