| Ejercicio 7 | |
|
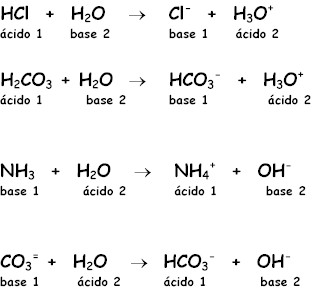
Aplicando la teoría de Brönsted-Lowry sobre ácidos y bases, explica el comportamiento de cada ion o molécula y las parejas ácido-base conjugado:
|
|
| Solución | |
|
Se
define ácido ®
cede iones H+ a una base.
Se define base ® capta iones H+ de un ácido.
HCl / Cl- H3O+ / H2O H2CO3 / -HCO3 (bicarbonato) NH4+ / NH3 H2O / OH- HCO3- / CO3= |
|